Volumetria de Complexação - Determinação de Ca e Mg
18.81k views3162 WordsCopy TextShare

Química Aplicada
Teoria e prática da determinação de Cálcio e Magnésio por volumetria de Complexação com EDTA. Assist...
Video Transcript:
o olá pessoal mais uma vídeo aula agora falando de uma outra aplicação volumétrica que a determinação de cálcio e magnésio na aula anterior do poder de neutralização a gente viu que o preparo de amostra eu peso cerca de um grama da minha amostra de calcário aplico ele é um ataque ácido no caso as clorídrico é deixe fervendo por cinco minutos essa solução obtida com o ácido remanescente a gente usou para determinar o poder de neutralização mas esse mesmo extrato eu posso fazer a determinação de cálcio e magnésio nela só que a gente para isso vai
fazer uma outra reação química até então a gente tava fazendo todas as reações do tipo ácido-base neste momento agora a gente vai fazer uma reação de complexação a complexação nada mais é do que uma reação química em que o produto é um complexo que seria isso é uma ligação em que envolve o metal e um agente ligante um agente ligante é um composto que tem lá é uma carga negativa o grupos funcionais com cargas negativos no qual se liga eletrostaticamente é essa a esse cátion que a gente tá envolvendo no nosso caso uma reação química
que a gente vai utilizar é a reação do edc aqui representado pelo y 4 - e o cálcio eo magnésio oedt ele é um agente complexante muito eficiente onde ele tem uma estabilidade química bastante grande com esses metais então a afinidade deles é bastante elevado na prática a gente vai utilizar a metodologia oficial do mapa para a determinação de cálcio e magnésio onde a gente e utilizou o mesmo procedimento de preparo de amostras seja um peso 1 grama de amostra adicionou 50 ml de um ácido clorídrico meio mal por litro ferver por 5 minutos obteve
um extrato de 100 ml e nesse estrato que a gente foi o mesmo que a gente utilizou poder de neutralização agora a gente vai fazer para determinação de cálcio e magnésio para isso a gente vai separar duas alíquotas uma alíquota de 5 ml para determinação de cálcio e uma outra líquida de 5 ml para determinação de cálcio + magnésio que que a gente vai colocar nesses animais no primeiro elenaria em que a gente vai fazer a determinação apenas de cálcio eu vou adicionar 50 ml de água simplesmente para aumentar um pouco volume 5 ml de
uma solução de k o h que tem como objetivo elevar o ph para aproximadamente 12 uma um a gente mascarante que é o cianeto de potássio 02 os outros a gente mas garante também que é trietanolamina vou colocar 6 gotas do indicador nesse caso aqui o indicador de complexação que ao com que tá na concentração de 0 5 porcento massa volume para o outro ele maia para determinação que a gente vai fazer de cálcio + magnésio é mais ou menos igual a única diferença é que em vez do hidróxido de potássio a gente vai colocar
uma solução tampão ph 10 e o indicador também muda porque aonde que a dor específico para o magnésio que é o eo cromo te ou negro de eriocromo t na 05 por cento também e aí eu vou titular com uma solução de edta 0,02 mol por litro é uma titulação comum a outra do ácido base só que agora eu vou titulando quando atingir o ponto final vai ocorrer a mudança de cor por conta dos o cálculo e ele o cromo tem mas por que que eu tenho que usar esses agentes mascarantes oedt ele é um
agente complexante muito eficiente ele reagir muito de forma muito eficiente com os metais só que ele não reage apenas com cálcio magnésio ele reage com todos os metais que a gente tem na cadeia aí e se a gente olhar essa figura é essa é a afinidade dos metais com edta cálcio e magnésio eles estão aqui no início ele tem uma baixa afinidade em relação a todos os outros metais e as mostras de calcários são amostras naturais são rochas são minerais né que contém esses outros metais aqui então o que que acontece no caso da titulação
do edc a com essas amostras caso esses metais estejam presentes na solução o sbt a que tem uma afinidade maior e como eles do que tem com cálcio e magnésio vão reagir preferencialmente com alumínio preferencialmente com cobre preferencialmente com ferro e assim por diante então antes do edc a reagir com cálcio e magnésio ele reagiria como esses elementos então o que que a gente precisa fazer eu preciso eliminar todos esses caras aqui antes de iniciar a titulação para determinar cálcio magnésio então como eu coloco ciamed potássio a treta lâmina eu estou reagindo e esses interferentes
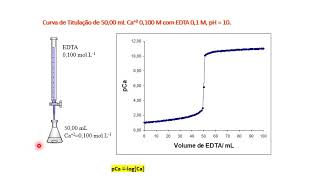
tô reagiram esses metais com cianeto com a trietanolamina e deixando-o livre cálcio e magnésio para titulação vamos entender um pouquinho o que tá acontecendo na reação de complexação né então vamos olhar a iniciar pela determinação de cálcio quando a gente tá falando hein na determinação de cálcio a solução a pagar aproximadamente 12 e se a gente for ver quais são as espécies químicas e como ela se comporta na solução ela teria mais ou menos esse perfil o cálcio e esse é o cálcio livre inicialmente ele tá sem por cento livre conforme eu vou colocando ele
terá ele vai complexando o ion cálcio vai sumindo da reação e e quando chegar mais ou menos no ponto de equivalência nesse caso aqui o nosso ponto final vai ser quando eu adicionar em torno de 10ml gta praticamente não existe mais cálcio livre todo cálcio vai estar complexado no caso aqui é a nossa concentração de editar no início todo editar que eu vou colocando vai reagindo com cálcio 1l vai sendo consumido e aí quando todo todos os metais tiverem complexados é isso sobra e de ti há no meio reacional no nosso caso e além do
cálcio na nossa mostra eu vou ter também outros elementos nesse caso aqui o magnésio vejo que a concentração do magnésio também começa lá né no seu máximo e aí conforme o ele te a vai entrando ele vai diminuindo a sua a sua concentração também né veja que o gta ele só vai sobrar né livre no meio como depois que ele completou todo o cálcio e todo o magnésio né outras espécies químicas também podem ser formadas e uma das mais críticas no caso aqui é o hidróxido de magnésio veja que quando eu tenho aqui em ph
12 que é mais ou menos a determinação que a gente vai deixar para o caos quando adiciona o cal h uma boa fração do magnésio né ele está na forma de hidróxido de magnésio então veja aqui e o magnésio ele vai caindo a sua concentração né mas é muito por ponta da formação do hidróxido de magnésio mais até do que da complexação de magnésio né da formação do complexo de magnésio esse é então vejam que o complexo cálcio eddga conforme a concentração de cálcio cai ela vai sendo aumentada a formação do complexo em cálcio e
de ter a mesma coisa acontece com a do magnésio né e de t a magnésio depois que todo isso aqui é importante depois que todo cálcio formou complexo com ele te a que vai começar a formação do complexo magnésio e de pentear então primeiro e determine o cálcio e depois eu continuar adicionando e de ter a ele vai complexar o magnésio no nosso caso e a nossa titulação que interessa nessa primeira condição é a determinação do cálcio apenas então o que a gente vai observar é isso a concentração de cálcio livre cai ea concentração de
edgar vai aumentando quando chegar nesse ponto aqui o nosso indicador vai mostrar para nós ele vai mudar de cor falando por isso que seguinte que todo cálcio livre desapareceu do meio reacional e aí então eu cheguei no meu ponto de equivalência ou ponto final nesse caso que o ponto final e quando eu tô falando agora do da determinação de cálcio + magnésio veja que o o o ph propositalmente foi ajustado para 10 com o uso de uma solução tampão a principal diferença dessa titulação para a titulação anterior do que a gente viu que era para
o somente para o cálcio e aqui cálcio magnésio é que na titulação anterior a gente viu que em ph12 mais ou menos a gente tinha uma grande formação do composto hidróxido de magnésio é que era a formação daquela daquele composto secundário quando eu ajusto ph para 10 essa espécie aqui que atrapalha a titulação porque ele forma um composto uma cinética mais mais lenta ele tem para era praticamente em expressivos e funções então em ph10 a concentração de magnésio que eu tenho majoritariamente ela está livre ela não tá né na forma de hidróxidos ela tá na
forma de magnésio livre isso é uma vantagem para titulação ela é importante para quem nossa situação aconteça então nesse caso a gente vai ter a formação então do complexo é cálcio edc e secundariamente a formação do complexo magnésio editar também é mas nesse caso agora o que importa para nós é a titulação do magnésio né eu quero quantificar quando tem do magnésio só que percebe que o cálcio tem uma afinidade com o dt a maior do que a do magnésio então eu não consigo eliminar o cálcio dessa minha titulação então o que que eu faço
eu título cálcio mais uma agnesio o edi te aqui tá sendo gasto aqui nessa titulação é o edc somado da complexação do cálcio e do magnésio e aí como que eu faço para determinar sol o valor do magnésio eu desconto a quantidade de editar que foi gasta na titulação do cálcio né então pô diferença é eu consigo determinar quanto é apenas para o magnésio então eu pego o meu valor total aqui nesse caso cálcio + magnésio e subtrai o valor do cálcio que o resultado na primeira naquele primeiro ele é maior que a gente viu
em quando a gente tava falando do das titulações ácido-base a gente viu que os indicadores tinham uma influência bastante grande nessa determinação aqui também vão ter mas como que funciona no caso do indicadores de complexação no caso dos ácidos ou bases ácidos e bases indicadores de ph eles são as moléculas indicadoras são ou ácidos ou bases no caso aqui no nos indicadores de complexação o nosso indicador é um agente ligante é um agente complexante no caso do cálcio o indicador é o cal com que essa estrutura molecular e quando em presença de um metal né
ele quando ele tá livre ele tem a cor azul né e quando em presença de um metal complexado ele se liga ao cálcio entra compartilhando aqui agora sua sua carga com esses grupos funcionais e essa cor muda para uma cor avermelhado um vinho quando eu coloco o meu indicador a gente indicador na solução imediatamente esse agente complexante vai se ligar ao cálcio e a solução então inicialmente vai ter cor avermelhada uma cor vinho oi e aí eu vou fazer a titulação eu vou colocar o edc a nessa minha solução o que que vai acontecer inicialmente
todo é de terá que tá sendo caindo gota gota ele não vai reagir com o meu o indicador ele vai pegar o calça que está livre né e levar e complexar o cálcio livre com ele te a formando um complexo cálcio e pth só que vai chegar o momento em que vai acabar ou é o cálcio livre da solução eu não vou ter mais calços disponível e aí o que que vai acontecer vai começar a ocorrer uma competição de estabilidade entre o edc aqui é um agente complexante e o cal com que a outra agente
complexante então o edc e o cal com eles vão ficar fazendo um cabo-de-guerra aí para ver quem consegue roubar o cálcio do outro como ele te a tem uma estabilidade muito maior do que o cal com o edt e aí roubaram o cálcio que tava ligado ao com e aí o cal cão perde aquela ligação metálica e volta seu estado inicial então aquela cor que era vinho inicialmente porque tava ligado ao mental quando o edgar roubou cálcio dela acaba voltando a cor azul e esse é o ponto de viragem e ao ponto em que a
gente vai perceber que é um momento de fechar a torneira e para a titulação a mesma coisa acontece com o élio cromo te o nego de hor eu prometer que vai ter um complexo com magnésio essa estrutura molecular do do negro de eriocromo t e aí aqui é a formação do complexo a cor também é vinho quando o edgar é entra também vai roubar o magnésio no nosso indicador e aí quando ele volta a sua fórmula inicial né a senha ligação no metal então a cor vai ser azul neve a fazer um exemplo aqui vamos
dizer que nossa titulação do branco tinha um pouco de cálcio na água e deu 0,2 ml titulei a minha mostra naquela solução preparada para o cálcio deu 10,2 ml o volume gasto então para complexar o cálcio né descontando o branco analítico seria o que eu gastei na minha titulação da mostra menos o branco então nesse caso 10,2 - 02 deu 10 mililitros eo numero de mols de dth nesse caso é a 0,2 mols em um litrão 1000ml se eu gastei 10ml eu vou gastar então 2 x 10 a menos 4 mols de editar só que
a gente viu que a relação estequiométrica entre cálcio e de ti a é de um para um então se isso que é o número de molde de tiara e a gente sabe que a relação de um-para-um eu posso falar que também é o número de mols de cálcio então esse é o número de mols de calça que eu tenho no meu ele é maia vou fazer a mesma coisa para o segundo a titulação que era cálcio + magnésio a situação do cálcio + magnésio deus 0,3 o branco a nossa amostra deu 15,0 vírgula 3 ml
diz contando o nosso branco dessa minha mostra deu 15 ml no total só que aqui ele o que é determinar o teor de magnésio então o que eu vou fazer eu vou subtrair o volume que dia de tiago que foi gasto para o cálcio né porque lembra que para esse pressa determinação o cálcio complexa primeiro com edc a e depois só o magnésio vai vai complexar e o ele é o cromo é um indicador apropriado né é específico para o magnésio então quando ele muda de cor é porque um magnésio foi roubado pela id&t a
então nesse caso eu posso simplesmente fazer a subtração do volume desse dessa mistura total pelo o volume indicar aos que a gente determinou no exemplo anterior então 15 - 10 é 5ml que é o volume de gta respectivo para o magnésio né ele somente o magnésio nesse caso tô fazendo a mesma regrinha de três 0,02 mol em um litrão 1000ml 5m o que é o respectivo para o magnésio é a gente vai ter um vezes 10 a menos 4 anos nesse caso também a relação magnésio é de ti a é de um para um então
se isso que é emoji e de t a é a mesma coisa para um monstro de genésio agora que a gente determinou quantos mols de cálcio e emoji magnésio eu tenho ele maia vamos descobrir qual é a porcentagem de cálcio e de magnésio que eu tenho na minha mostra como que a gente vai fazer essa conta primeira coisa a gente tem que olhar o procedimento procedimento foi o seguinte diz aí um grama de calcário coloquei lá uma quantidade de ácido ajustei isso por um volume de 100 ml então eu tenho um grama em 100 ml
da amostra tirei a alíquota de 5 ml dessa desse meu extrato de 100 e coloquei no meu né maia então não é maia ea titulação que você fez um número de mols que você se determinaram é de estar e não de 5ml desse extrato então vamos descobrir quanto da minha mostra eu tenho lá na alemanha então uma regra de três simples se eu tenho um grama da minha amostra em 100 mililitros numa porção de 5ml que eu tô colocando aqui dentro teria quanto 0,05 tão teoricamente né essa minha amostra de calcário aqui que eu peguei
esse um grampo coloquei e sem só que depois eu peguei só 5 ml da solução e coloquei aqui ela tá me transferindo 0,05 g da minha mostra para esse frasco para essa porção aqui né então teoricamente eu tenho né 2 x 10 a menos 4 mols de cálcio em 0,05 g da minha mostra então eu em cinco emieles aquela massa e eu vou fazer uma regrinha de três agora a 0,05 gramas de amostra tem 2 vezes 10 a menos 4 mols de cálcio a minha relação percentagem vai ser em função da massa então eu vou
converter esse número de mós em massa que que eu como que eu faço isso eu sei que o molde calça é 40 então esse número de mós vai ser isso 8 x 10 a menos 3 g de cálcio como eu quero uma relação percentual eu vou fazer para 100 gramas na minha mostra então 0,05 está para 2 vezes 10 a menos 4 ou 8 x 10 a menos 3 gramas e 100 gramas eu tenho x isso o x me dá 16 gramas ou seja 16 em sem eu tenho 16 por cento de cálcio a mesma
coisa eu faço para o magnésio né então eu tenho um vezes 10 a menos 4 mod magnésio sabendo que a massa atômica do magnésio é 24 eu vou ter 2,4 e no - 3g de magnésio para 100 gramas de estudar 4,8 ou 4,8 por cento então a partir dessa titulação a partir dessa determinação dos volumes de dth sus nessa nessa nariz a gente conseguiu determinar o teor de cálcio e o teor de magnésio naquela amostra de calcário que a gente tinha então essa mesma amostra de calcário o que for utilizado para análise do pn também
pode ser utilizado para determinação de cálcio e magnésio tá certo pessoal vejam aí o vídeo prático como é realizado verdadeiramente um grande abraço tchau tchau o que significa isso e aí e aí e aí e aí e aí e aí e aí e aí e aí e aí e aí e aí e aí e aí e aí e aí
Related Videos

31:42
Determinação de Carbono Orgânico - Método ...
Química Aplicada
6,691 views

20:56
Fundamentos da Volumetria
Química Aplicada
12,454 views

37:21
Gravimetria
Química Aplicada
23,018 views

18:17
Procedimento de Padronização
Química Aplicada
25,843 views

21:59
Tudo sobre Titulação #7 Titulação de Compl...
Universidade da Química
87,033 views

42:52
Erro em análise química
Química Aplicada
7,726 views

10:13
TITULAÇÃO COM EDTA
Química Tarja Preta
29,563 views

58:14
Amostragem para análise química
Química Aplicada
8,893 views

30:33
Tudo sobre Titulação #1 Titulação de Ácido...
Universidade da Química
129,513 views

18:11
Volumetria de Complexação - Determinação ...
André Cera - Aulas Práticas de Química
7,106 views

22:43
Extrações assistidas por ondas ultrassônicas
Química Aplicada
1,695 views

52:27
TITULAÇÃO ÁCIDO BASE - TEORIA E EXERCÍCIOS
QUÍMICA DO MONSTRO
128,384 views
20:56
Volumetria de complexação (Aula 1)
Pedro Orival Luccas
4,129 views

26:38
Titulação de acido base com o prof. Guilhe...
Prof. Guilherme Química
134,354 views

37:00
Química Analítica Experimental 2: Volumetr...
Rafael de Queiroz Ferreira
4,716 views

14:48
Tudo Sobre Química Analítica - Titulação p...
Universidade da Química
11,491 views

15:48
#QUÍMICA - TITULAÇÃO PARTE 1
Coltec Tube
40,320 views

16:32
Química Analítica Experimental 2: Volumetr...
Rafael de Queiroz Ferreira
3,865 views

46:16
Preparo da amostra por Via Umida
Química Aplicada
2,631 views

13:03
Volumetria de precipitação
Farmácia Descomplicada
13,350 views