COMO FAZER BALANCEAMENTO DE EQUAÇÕES QUÍMICAS
824.42k views892 WordsCopy TextShare
Estuda Mais
🛑Seja um membro do canal do Estuda Mais e receba diversos benefícios do canal: https://www.youtube....
Video Transcript:
o Olá pessoal tudo bom com vocês aqui é o professor Gabriel zaid do canal de estudar mais e vamos começar por aqui a resumo saúde mais um exercício de química mas não esqueça de se inscrever aqui no nosso canal no YouTube e deixar um like nesse vídeo caso você goste do nosso conteúdo e hoje a gente vai resolver esse balanceamento de equações químicas bom para resolver um balanceamento você tem que igualar a quantidade de ácidos que você tem do lado dos reagentes e do lado dos produtos de uma equação aqui do lado dos reagentes nós
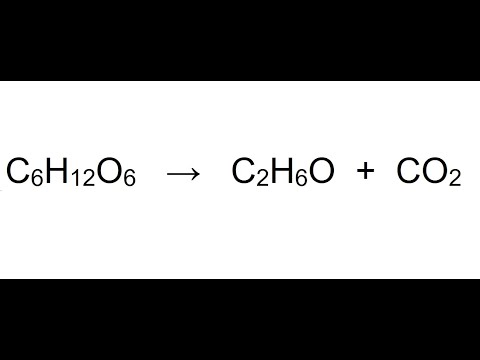
temos seis átomos de carbonos 12 átomos de hidrogênio e seis átomos de oxigênio então nós temos três elementos químicos que são o elemento carbono e o elemento hidrogênio é o elemento oxigênio e com relação ao número de átomos de cada elemento o salto 6 12 e 6 e esses números você encontra na frente dos seus atos dentro da molécula que eu tenho de glicose O que foi decomposto em um álcool e os jogos carbono a gente tem seis átomos de carbonos 12 hidrogênios e seis átomos de oxigênio Então tá aqui o a quantidade que a
gente tem que cada um dos lados Agora do lado e produtos só tem os mesmos elementos carbono hidrogênio e oxigênio Quantos carbonos eu tenho do lado dos produtos você poderia estar olhando aqui de série e falavam tenho dois né Professor mas na verdade não porque os produtos são todas as moléculas que a gente tem Depois dessa certinha então no caso eu tenho dois aqui mais um aqui então no total a gente tem três átomos de carbonos com relação aos hidrogênios eu só tenho nessa primeira molécula então só tenho esses seis aqui mesmo oxigênio Eu tenho
um aqui mais dois aqui então no total são três oxigênio você já deve ter percebido que quando eu tenho o número um como índice a gente não mandar um curso muito locais número um e a gente deixa sem ele tá então beleza agora o que que é diferente a quantidade de oxigênio está diferente a de hidrogênio EA de carbono para gente Balancear a quantidade de carbonos por exemplo eu poderia aumentar a quantidade duas vezes de carvão do lado dos produtos para ficar igual ao seis carbonos que eu tenho do lado que a gente isso dá
para fazer colocando um número dois aqui esse dois Vai Multiplicar pela quantidade de carbonos duas vezes dois vão ser quatro mais um tá sendo igual a cinco próxima então dá para aumentar mais dá para aumentar mais só que eu tenho que aumentar deste lado aqui porque porque esse dois e também multiplica pela quantidade de hidrogénio joga que acontece duas vezes seis são 12 então eu acabo igualam dos hidrogênios colocando esses dois aqui e a equação para o hidrogênio já ficou balanceado não se aumentar a colocação e aqui na frente do meu álcool e eu desbalancear
hidrogênio então eu vou colocar um dois na frente do CO2 assim é você duas vezes um dois a dois carbonos mais aqueles quatro carbonos vamos centralizar seis carbonos se a gente colocar o coeficiente sei que o médico dois na frente do dióxido de carbono então aqui a nossa equação para o carbono e para o hidrogênio a gente já nota que estão balanceadas bom agora é só vai faltar a gente conferir para ver se para o oxigênio é equação também ficou balanceado então com relação aos higiene eu tenho duas vezes um são dois duas vezes dois
que são 44 com mais dois são seis então a gente tem seis oxigênio solados produtos e os lados reagentes Também logo a gente percebe que a equação química foi balanceada de forma correta bom pessoal basicamente isso quando a gente faz um balanceamento de equações químicas o que importa para gente são os coeficientes estequiométricos que são esses números que a gente se coloca na frente das moléculas no caso do da glicose não coloquei nada aqui na frente você pode colocar o número um com 805 médico para ela tá então se o professor pede para você faça
o balanceamento de equações você não precisa fazer tudo isso que eu coloquei aqui embaixo Isso é só um rascunho para vocês irem tem dela ser alta mesmo pode fazer também o rascunho mas o balanceamento em si É só colocar esses coeficientes estequiométricos na frente da das moléculas e esses coeficientes multiplicam pela quantidade de ácidos que a gente tem dentro de cada molécula deixado igual o lado dos reagentes e dos produtos a equação está balanceada corretamente tá bom é isso pessoal eu vou ficando por aqui a gente termina mais uma vídeo aula de balanceamento de equações
químicas que você quiser praticar se você quiser resolver outras questões de balanceamento de equações dá uma olhada na descrição desse vídeo que eu deixei é uma playlist o jogo esse vídeo Faz parte com várias balanceamento de equações químicas tanto pelo método da tentativa e erro quanto pelo método da oxirredução tá bom e futuramente também vou postar aqui do canal balanceamento uma playlist balanceamento de equações químicas pelo método ion elétron então fiquem espertos aí fiquem ligados a gente vai se encontrar na nossa próxima aula forte abraço tchau tchau
Related Videos

10:14
Balanceamento de Equações Químicas
Estuda Mais
215,942 views

48:35
IMPOSSÍVEL NÃO APRENDER BALANCEAMENTO DE E...
Diego Fares
72,096 views

8:59
BALANCEAMENTO DA EQUAÇÃO QUÍMICA: FeCl3 + ...
Estuda Mais
85,166 views

12:25
✍🏼Como calcular número de oxidação: NOX.
Química com Flávio
6,854 views

7:59
🧪 BALANCEAMENTO POR TENTATIVAS: APRENDA R...
Professor Gabriel Cabral
450,383 views

6:40
Como fazer balanceamento de equações químicas
Estuda Mais
88,368 views

15:44
Portugal VS Brazil l Which Portuguese is E...
World Friends
422,146 views

6:59
Como Interpretar QUALQUER Equação Química
Ciência Mapeada
99,862 views

8:51
Balanceamento de equações: NH4Cl + Ba(OH...
Estuda Mais
43,217 views

9:25
Entenda a TABELA PERIÓDICA em 10 minutos -...
Toda Matéria
1,702,237 views

11:01
9º Ano - Química - Aula 13 - Reações quími...
Mitocôndria
244,664 views

9:03
Como fazer balanceamento de Equações Químicas
Estuda Mais
109,584 views

17:37
George Simion, față în față cu Andreea Esc...
Știrile ProTV
89,283 views

27:27
Balanceamento de reações químicas - exercí...
Uma Dose de Química
214,138 views

38:08
Tutunul încălzit e sigur sau…? Știi ce îns...
Starea Sănătății
22,239 views

8:03
REAÇÕES Químicas - EQUAÇÕES Químicas
KiFacil
79,846 views

17:21
Why Franch is so different? Pronunciation ...
World Friends
367,537 views

7:44
BALANCEAMENTO DE EQUAÇÕES QUÍMICAS
Estuda Mais
44,823 views

21:31
What's Your ENGLISH LEVEL? Take This Test!
Brian Wiles
2,591,105 views